Kundenreferenzen
Universität Washington: Zwei-Laser-Multiphotonenmikroskop für die Immunologie und andere Forschungsbereiche
Herausforderung
Dr. Mark Miller ist außerordentlicher Professor und Direktor des Zentrums für In-vivo-Bildgebung an der Medizinischen Fakultät der Washington University in St. Louis. Er verfügt über umfangreiche Erfahrung in der Herstellung und dem Einsatz von Multiphotonenmikroskopen, insbesondere hinsichtlich der Anwendung dieser Technologie in der Immunforschung an lebenden Organismen. Dazu gehören bahnbrechende Arbeiten zum Transport von Leukozyten und zur Antigenpräsentation sowie neue Anwendungen in der computergestützten Biologie. So hat sein Team beispielsweise erstmals gezeigt, dass T-Zell-Populationen, die an APCs (Antigen-präsentierende Zellen) binden, nicht durch Chemokine-Gradienten gesteuert werden, sondern ihre Bewegung zufällig beginnen (Miller et al., Science, 2002; Miller et al., PNAS, 2004; Miller et al., JEM, 2004).
Seit 2012 ist er zudem Leiter der Abteilung für In-vivo-Bildgebung. In dieser Abteilung hat er ein universell einsetzbares Multiphotonenmikroskop entwickelt, das interdisziplinären Forschern für die Einzelzellbildgebung bei der Erforschung von Infektionskrankheiten in lebenden Organismen zur Verfügung steht. Entscheidend für den Bau dieses Mikroskops war die Notwendigkeit zweier unabhängig voneinander einstellbarer Laser (Zinselmeyer et al., Methods in Enzymology, 2009), um flexible Experimente mit mehreren Fluoreszenzfarbstoffen zu ermöglichen. Außerdem mussten die Laser benutzerfreundlich sein, um ein breites Anwenderpublikum zu unterstützen, und eine hohe Zuverlässigkeit aufweisen, um eine effiziente Mehrbenutzer-Planung zu ermöglichen.
Lösung
Dr. Miller entschied sich schließlich dafür, ein handelsübliches Mikroskop umzurüsten und es mit zwei Chameleon II-Lasernauszustatten, unter anderem weiler bereits in seinem Immunologielabor mit Chameleon gearbeitet hatte und überumfangreiche Erfahrungen damit verfügte. Er fügte hinzu, dass er sich für den Vision II entschieden habe, da diese Modelle den größten direkten Abstimmbereich bei den Titan-Saphir-Lasern bieten. „Dies bietet unseren Kooperationspartnern ein umfassendes Spektrum an Anregungswellenlängen, darunter 800 nm für Spontane Fluoreszenz, 900 nm für grüne (und blaugrüne) Fluoreszenzproteine sowie 1040 nm für die roten Fluoreszenzproteine der mfruit-Serie. Die längeren Wellenlängen tragen zudem dazu bei, Spontane Fluoreszenz und Lichtschäden bei In-vivo-Gewebeexperimenten mit längeren Belichtungszeiten auf ein Minimum zu reduzieren.“
Dr. Miller wies darauf hin, dass der innovative Kundendienst ein weiterer entscheidender Faktor für seine Wahl dieses Lasers war. „Bei der Nutzung früherer Lasermodelle sind wir auf einige Probleme gestoßen. Coherent jedoch Coherent , die Leistung des Lasers wieder auf 100 % des Neuzustands zu bringen; die einzige Ausfallzeit war praktisch nur die Zeit, die benötigt wurde, um den Ersatzlaser in mein Labor zu liefern.“ Obwohl er volles Vertrauen in den Vision II-Laser hat, erklärt er, dass der Vertrag dennoch ein „beruhigendes“ Kundendienst-Erlebnis biete und einen unterbrechungsfreien Versuchsbetrieb garantiere.
Ergebnisse
Dr. Miller erklärte, dass das Doppellaser-Mikroskop in Bezug auf Leistung, Zuverlässigkeit und Benutzerfreundlichkeit ein großer Erfolg sei; neue Anwender benötigten in der Regel nur wenige Stunden praktische Einweisung, um das System bedienen zu können. Das Gerät hat bereits Daten für Veröffentlichungen zu Dutzenden verschiedener Themen geliefert. Dr. Miller hat auf YouTube eine beeindruckende Präsentation veröffentlicht, die zahlreiche Bilder und Videos enthält, welche seine langjährige Erfahrung mit der In-vivo-Multiphotonen-Bildgebung dokumentieren.
Literaturverzeichnis:
Zweiphotonen-Bildgebung der Lymphozytenmotilität und der Antigenreaktion in einem intakten Lymphknoten.
Miller MJ, Wei SH, Parker I, Cahalan MD. Science. 7. Juni 2002;296(5574):1869–73. doi: 10.1126/science.1070051. Online-Veröffentlichung: 16. Mai 2002.
Das Durchsuchen des T-Zell-Repertoires wird durch das dynamische Verhalten dendritischer Zellen und die zufällige Motilität der T-Zellen im Lymphknoten gefördert. Miller MJ, Hejazi AS, Wei SH, Cahalan MD, Parker I. Proc Natl Acad Sci U S A. 27. Januar 2004;101(4):998-1003. doi: 10.1073/pnas.0306407101. Online-Veröffentlichung: 13. Januar 2004.
Darstellung der Einzelzelldynamik der CD4+-T-Zell-Aktivierung durch dendritische Zellen in Lymphknoten.
Miller MJ, Safrina O, Parker I, Cahalan MD. J Exp Med. 4. Oktober 2004;200(7):847-56. doi: 10.1084/jem.20041236.
Kapitel 16. Zwei-Photonen-Mikroskopie und mehrdimensionale Analyse der Zelldynamik.
Zinselmeyer BH, Dempster J, Wokosin DL, Cannon JJ, Pless R, Parker I, Miller MJ.
Methods Enzymol. 2009;461:349–78. doi: 10.1016/S0076-6879(09)05416-0.
„Dank des innovativen Servicevertrags besteht die einzige Ausfallzeit praktisch nur aus der Zeit, die benötigt wird, um den Ersatzlaser in mein Labor zu liefern.“
— Mark Miller, außerordentlicher Professor an der Medizinischen Fakultät der Washington University (St. Louis)


Abb. 1. Maßgeschneidertes Zwei-Photonen-System von WashU IVIC
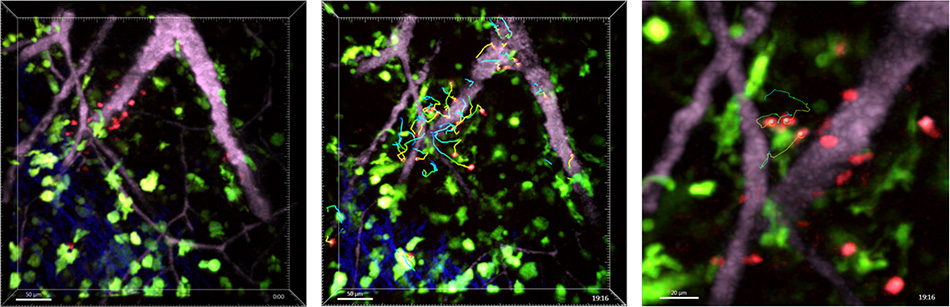
Abb. 2:Die in vivo-Zweiphotonen-Bildgebung der „Antigenerkennung durch T-Zellen“zeigt die entscheidende Rolle, die die zufällige Bewegung der T-Zellen bei der Auslösung der adaptiven Immunantwort spielt. T-Zellen (rot) wandern aus den kleinen Venen mit dichtem Endothel (rosa) in den Halslymphknoten aus und kommen dort zufällig mit dendritischen Zellen (grün, vergrößerte Ansicht) in Kontakt.