Artikel
Zukunftsorientierte hochauflösende 3D-Bildgebung mit mehreren Wellenlängen
Das innovative SCAPE-Mikroskop (Scanning Confocal Planar Excitation) mit Laser-Fluoreszenz-Technologie
überwindet die Einschränkungen früherer Verfahren und bietet vielfältige Anwendungsmöglichkeiten in den Biowissenschaften.
Überblick
Forscher aus verschiedenen Bereichen der Biowissenschaften haben gemeinsame Anforderungen an 3D-Fluoreszenzmikroskope: Diese Mikroskope zeichnen sich durch hohe Geschwindigkeit, hohe Bildauflösung und Einzelzellauflösung aus und ermöglichen die Aufnahme von Bildern, ohne dass die Proben nennenswerten Lichtschäden ausgesetzt werden. Doch trotz enormer Fortschritte und technischer Verbesserungen erfordern die meisten ausgereiften Technologien nach wie vor Kompromisse, sodass unvermeidlich Abstriche bei mindestens einem dieser Parameter gemacht werden müssen.
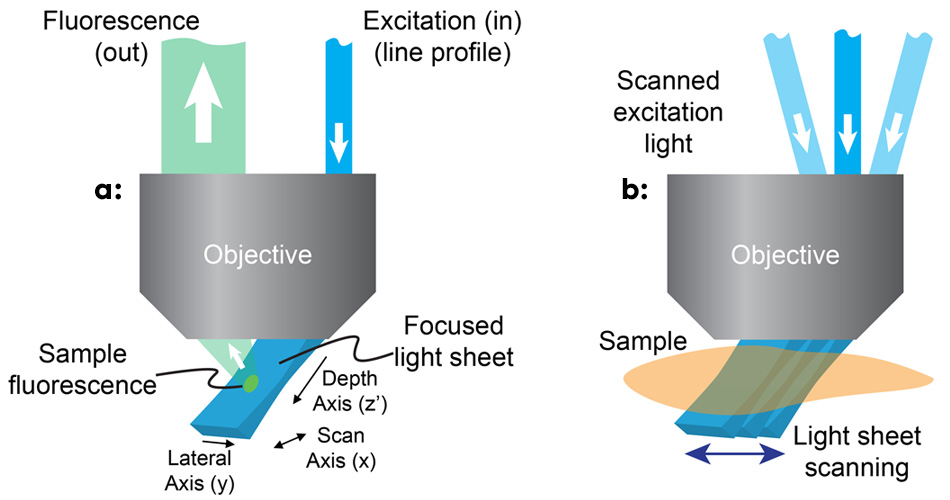
Abb. 1:Bei SCAPE wird das Objektiv des Hauptmikroskops durch einen linienförmigen Lichtstrahl außeraxial bestrahlt, wodurch ein Lichtstreifen unter einem schrägen Winkel entsteht (a); SCAPE erstellt ein Volumenbild, indem es diesen Lichtstreifen abtastet und dabei eine Reihe von Bildern der bestrahlten Ebene aufnimmt (b).
Fortschritt und Abwägungen
Beispielsweise istes bei der konfokalen Mikroskopieaufgrund der Geschwindigkeitsbeschränkungen beim physikalischen Abtasten einzelner Lichtpunkte nicht möglich, große xyz-Volumen mit hoher Auflösung bei einer variablen Wiederholfrequenz abzubilden. Zudem ist die Verweildauer pro Pixel sehr kurz, was bedeutet, dass selbst die schnellsten konfokalen Abtastungen eine hohe Laserleistung erfordern, was zu erheblichen Lichtschäden an lebenden Proben führt.
Obwohldie Zwei-Photonen-MikroskopieLichtschäden deutlich reduzierenkann, steht auch dieses Punktabtastverfahren vor dem gleichen Problem, nämlich dem Kompromiss zwischen Geschwindigkeit, Auflösung und Volumen. Kürzlich entwickelte schnelle akusto-optische Modulatoren (AOM) können vorab ausgewählte kleine Volumina schneller abtasten, doch ist diese Methode für große Volumina oder sich bewegende Lebewesen nur begrenzt einsetzbar.
Herkömmliche Lichtscheibenmikroskope können die gesamte xy-Ebene gleichzeitig abtasten, erfordern jedoch eine laterale Abtastung (und damit eine spezielle Vorbereitung) und benötigen Zeit, um einen 3D-Datenwürfel zu erstellen. Darüber hinaus machen die Synchronisation der Bewegungen von Optik und Objekttisch diese Techniken komplex und langsam.
Professorin Elizabeth Hillman vom Zuckerman Mind Brain Behavior Institute der Columbia University (New York City, New York) und ihre Kollegen machten sich daran, einen innovativen Ansatz zu entwickeln, um diese Einschränkungen zu umgehen und gleichzeitig Proben in verschiedenen Formen – sowohl in Kapseln als auch ohne Kapseln – zu untersuchen. Schließlich gelang es ihnen, das SCAPE-Mikroskop (Scanning Confocal Plane Excitation) zu entwickeln,das erstmals 2015 in einer Veröffentlichung vorgestellt wurde.1 Im Jahr 2019 wurde eine aktualisierte Version, SCAPE 2.0, vorgestellt,2 und LeicaMicrosystems hat die vielfältigen Anwendungsmöglichkeiten in den Lebenswissenschaften erkannt und nun eine Lizenz für dieses Mikroskop erworben.
So funktioniert SCAPE
Hillman erklärte: „Wir gingen davon aus, dass eine Einzelpunkt- oder sogar Mehrpunktabtastung niemals eine wirklich schnelle Bildgebung ermöglichen würde. Selbst wenn wir die erforderliche Abtastgeschwindigkeit erreichen könnten, wäre die Verweildauer pro Pixel zu kurz, um Bilder mit einem akzeptablen Signal-Rausch-Verhältnis zu erhalten.Deshalb begannen wir, uns mit der Lichtblattmikroskopie zu beschäftigen. Damals benötigten fast alle Systeme zwei Objektive, die im 90°-Winkel zueinander um die Probe angeordnet waren. So stellte sich die Frage: Können wir die Vorteile der Lichtblatttechnik mit mehreren Pixeln in eine Konfiguration mit nur einem Objektiv integrieren?“
Das Team erkannte, dass die Verwendung eines außeraxialen Strahlengangs am Rand eines Objektivs mit hoher numerischer Apertur einen Anregungslichtfleck bildet, der in einem Winkel von 45° zur tatsächlichen xy-Ebene des Mikroskops liegt (siehe Abbildung 1). Um die Fluoreszenz von dieser schrägen Ebene abzubilden, drehten sie die Bildebene des Objektivs und fokussierten die Kamera präzise nach einer Methode, die der des schrägen-Ebenen-Mikroskops ähnelt.3 Hillman und ihr Team bewegten den Lichtfleck mithilfe eines vor dem Objektiv angeordneten Scanspiegels von einer Seite zur anderen, wodurch auch die zurückkehrende Fluoreszenz umgelenkt wurde, sodass der Fokus auf dem sich bewegenden Lichtfleck blieb. Durch die Überlagerung der Ebenen während der Bewegung des Scanspiegels kann das Mikroskop schnell und wiederholbar dreidimensionale Volumenbilder erzeugen.
Einige Details von SCAPE 2.0 (siehe Abbildung 2) bedürfen einer Erläuterung. Das Problem der schrägen Bildgebung (d. h. der Lichtscheibe, die in einem bestimmten Winkel zur Betrachtungsachse steht) wird gelöst, indem das über einen Zwischenobjektiv aufgezeichnete Fluoreszenzlicht an einem Zwischenpunkt ein tatsächlich schräg stehendes Bild erzeugt. Dieses Bild wird dann durch ein zweites Objektiv erfasst, das in einem bestimmten Winkel (etwa 127°) angeordnet ist, um die Ebene der Lichtscheibe horizontal auf die Kamera zu fokussieren.
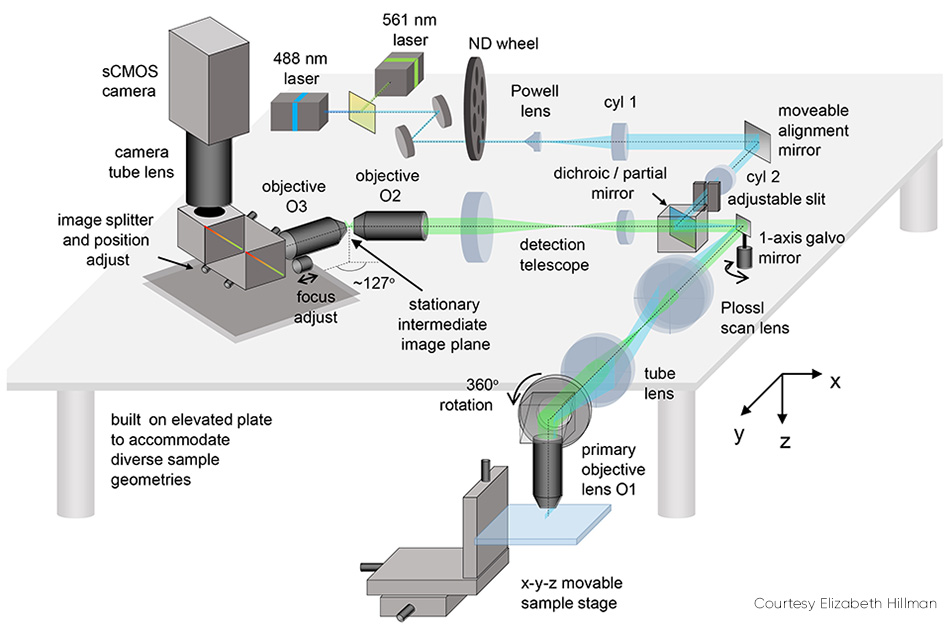
Abb. 2:Der bewegliche Kalibrierungsspiegel ist eine der Schlüsselkomponenten von SCAPE 2.0.
Das endgültige Bild auf der Kamera zeigt eine schräge y-z-Ebene innerhalb der Probe, die in der Regel rechteckig ist; da das Licht die meisten Gewebe nur begrenzt durchdringen kann, ist diese Ebene in z-Richtung (relativ zur y-Richtung) schmaler. Bei solchen Proben ist es sinnvoll, die Kamera so zu betreiben, dass sie nur eine geringere Anzahl von Zeilen (entsprechend der Tiefe in z-Richtung) erfasst, da dies eine schnellere Bildgebung ermöglicht.So können beispielsweise je nach verwendeter Kamera 200 Zeilen mit einer Geschwindigkeit zwischen 1000 und 18.000 fps ausgelesen werden.
Durch den Einsatz eines Mehrfachspiegels zum Abtasten der Lichtscheibe konnte das Problem der Abtastsynchronisation erstmals gelöst werden. Der Detektionsweg umfasst die Fläche, die an die für das Anregungslicht verwendete Fläche angrenzt. Hillman erklärt: „Dieser Mehrfachspiegel war die ursprüngliche Inspiration für SCAPE, doch wir erkannten schnell, dass die Verwendung eines einzelnen Schwingspiegels einfacher und ebenso effektiv sein würde. Diese Änderung macht die Herstellung des Systems einfacher und kostengünstiger, lässt mehr Licht zur Kamera zurückkehren und erleichtert die Steuerung des Abtastmodus des Systems.“
Da es außer dem Scankopf keine weiteren beweglichen Teile gibt, wird die Gesamtgeschwindigkeit von SCAPE lediglich durch die Bildrate der Kamera und das Signal-Rausch-Verhältnis (SNR) begrenzt. Je nach Experiment entspricht das Scannen des Scankopfes mit einer Frequenz von 10 bis 100 Hz einer beispiellosen Volumenrate von 10–100 Vol/s (vps). SCAPE verwendet einen herkömmlichen Sägezahn-Scanmodus,d. h. nach dem linearen Scan erfolgt ein quasi-sofortiger Reset. Der Scanbereich des Scanner-Spiegels und die Anzahl der Kamerabilder pro Scan bestimmen das Sichtfeld des Systems und die Abtastdichte in x-Richtung. Durch den Einsatz schnellerer Kameras lassen sich die Volumenrate, die Abtastdichte oder das Sichtfeld verbessern. Obwohl das Team für den Großteil der Bildgebung Standard-sCMOS-Kameras verwendet, gelang es ihnen mit ultraschnellen CMOS-Kameras mit integriertem Verstärker, Bildraten von über 300 vps zu erreichen.
Da die gescannten Bildscheiben in einem bestimmten Winkel zur Bildbetrachtungsachse z stehen, ist jede Tiefenscheibe gegenüber der nächsten leicht versetzt. Der Computer des Mikroskops korrigiert diese „Neigung“ mithilfe einfacher Transformationen und erzeugt so ein verzerrungsfreies 3D-Bildvolumen.
Digitale Lasermodulation
Durch die gleichzeitige Beobachtung mehrerer Fluoreszenzmarker (einschließlich funktioneller Indikatoren und Fluoreszenzproteinen) lassen sich kinetische Vorgänge (wie beispielsweise Muskelbewegungen) mit der molekularen Zusammensetzung, der Zellstruktur und neuronalen Signalen in Zusammenhang bringen. SCAPE ermöglicht durch den plugg-and-play-fähigen Coherent (OPSL) eine Anregung mit mehreren Wellenlängen und unterstützt so problemlos solche Anwendungen. Optional können zwei oder mehr spektral getrennte Bilder gleichzeitig nebeneinander auf der Kamera erfasst werden.
Hillman wies auf mehrere innovative Vorteile der OPSL-Technologie im Vergleich zu früheren Lasertypen in dieser Arbeit hin. Sie hob die Vielfalt der verfügbaren Wellenlängen und Leistungsstufen hervor. „Vor einigen Jahren standen uns, wenn es um die verfügbaren Leistungsstufen ging, lediglich 488 nm, 532 nm und 638 nm zur Verfügung – das war so ziemlich alles. Im gelben und orangefarbenen Bereich hatten wir keine andere Wahl.Heute können wir jedoch zwischen Laserquellen mit Leistungen von einigen Dutzend bis zu einigen Hundert Milliwatt wählen, deren Wellenlängen präzise auf die Anregung fast aller gängigen Fluoreszenzfarbstoffe abgestimmt sind.“ Sie erklärte, dass die meisten ihrer SCAPE-Systeme mehrere Freiraumlaser integrieren, was ihnen eine höhere Flexibilität als bei fasergekoppelten Systemen bietet. „Die Laser sind kompakt, haben alle genau die gleichen Abmessungen und verfügen über identische elektronische Schnittstellen, was die Handhabung sehr vereinfacht.“ Hillman sagt, dass sie bisher in einigen Experimenten bereits bis zu fünf Laserwellenlängen verwendet haben. Sie erklärt außerdem, dass sie SCAPE häufig zu Workshops und Schulungen mitbringt und die verfügbaren OBIS-Laser verwendet, die nur selten neu kalibriert werden müssen.
Die digitale Bildgebung ist eine weitere wichtige Funktion von OPSL-Lasern. Da sich OPSL-Laser mit einer Frequenz von bis zu 25 kHz ein- und ausschalten lassen,kann die Anregungswellenlänge in zeitlich präzise abgestimmten aufeinanderfolgenden Bildfeldern wechseln. Diese Funktion lässt sich durch die Verwendung eines im Labor gebauten Bildteiler (bestehend aus einem dichroitischen Filter und einem Filter) für die Mehrwellenlängen-Detektion ergänzen. Das Gerät projiziert spektral getrennte Bilder mit einem Sichtfeld von bis zu 1280 Voxeln, ohne dass dies Auswirkungen auf die Bildgebungsgeschwindigkeit im Vergleich zum Einwellenlängenbetrieb hat.
Kompetenzen und Leistungsspektrum
Zwei aktuelle Kooperationsprojekte verdeutlichen die Leistungsfähigkeit und den Anwendungsbereich von SCAPE.
Die Bildgebung kleiner Organismen (einschließlich des gesamten Körpers, des Gehirns und des Nervensystems) ist ein Trend in den Neurowissenschaften.Hillman und seine Kollegen haben kürzlich eine Studie veröffentlicht, in der sie ihre Hochgeschwindigkeits-3D-Bildgebung von genkodierten und kalziumempfindlichen Fluoreszenzproteinen in lebenden Fruchtfliegenlarven beschreiben (siehe Abbildung 3). Neben der Erfassung der komplexen dynamischen Eigenschaften des Körpers und des Nervensystems der Larven während der peristaltischen Fortbewegung verfolgte das Team auch die Entladungsmuster der entlang der Körperwand verteilten Neuronen während der Deformation.
Das Team untersuchte mithilfe von SCAPE zudem die dynamischen Entladungsprozesse von Neuronen in der Großhirnrinde lebender Nagetiere 5 sowie von olfaktorischen Riechnervenzellen in der Nase von Mäusen 6 und führte Bildgebungsaufnahmenanfrei beweglichenCaenorhabditis elegans-Fadenwürmern durch. Darüber hinaus erstellten sie eindrucksvolle Videos vom Herzschlag von Zebrafischembryonen. 2
Die Untersuchung des Herzens von Zebrafischembryonen ermöglicht tiefe Einblicke in die Herzentwicklung von Wirbeltieren, einschließlich der Auswirkungen genetischer und umweltbedingter Faktoren auf Struktur und Funktion. Herkömmliche mikroskopische Analysen erfordern zeitliche Selektion, was bei einer natürlichen Herzfrequenz von 2 bis 4 Hz unweigerlich dazu führt, dass Details wie unregelmäßige Herzrhythmusstörungen übersehen werden, und es ist nicht möglich, rote Blutkörperchen (RBC) eine vollständige 4D-Partikelverfolgung durchzuführen. Das Team um Hillman arbeitete mit der Kinderkardiologin Prof. Kimara Targoff zusammen, deren Labor Zebrafische nutzt, um Genmutationen zu entschlüsseln, die zu Herzfehlbildungen bei Embryonen führen können. Im Rahmen dieser Zusammenarbeit nahmen sie Videos von roten Blutkörperchen während des Herzschlags mit einer Bildrate von über 100 vps aufund erfassten mithilfe von GCaMP-Markern einzelne Wellenformen der Kalziumaktivität über den gesamten Herzschlag hinweg (siehe Abbildung 4).
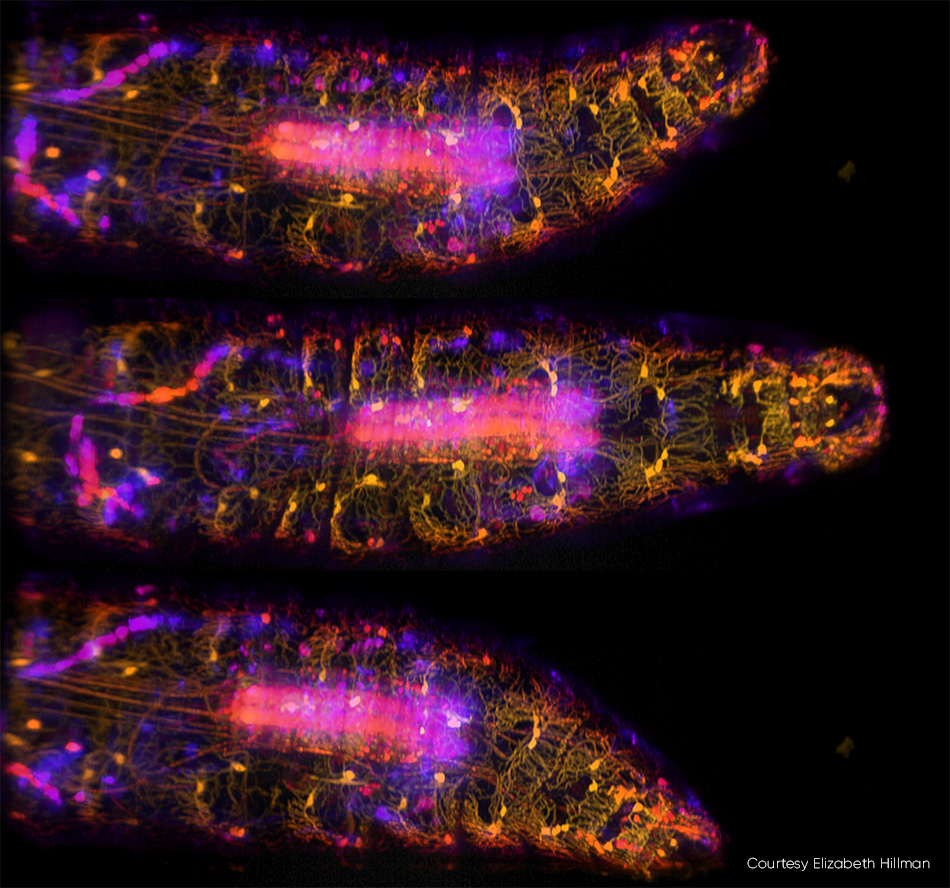
Abbildung 3:In diesen drei Bildern von sich bewegenden Fruchtfliegenlarven, die mit SCAPE 2.0 mit einer Bildrate von 10 vps aufgenommen wurden [3], wurden die ventralen somatosensorischen Neuronen mit GFP markiert und mit einer 488-nm-Anregung abgebildet.Die Farben (von Gelb bis Blau) stehen für Signale, die aus unterschiedlichen Tiefen der Probe stammen. Weitere Informationen finden Sie in der Studie von R. Vaadia et al. [4]; eine Echtzeit-Videosequenz zu dieser Studie finden Sie unter http://bit.ly/SCAPE2019.
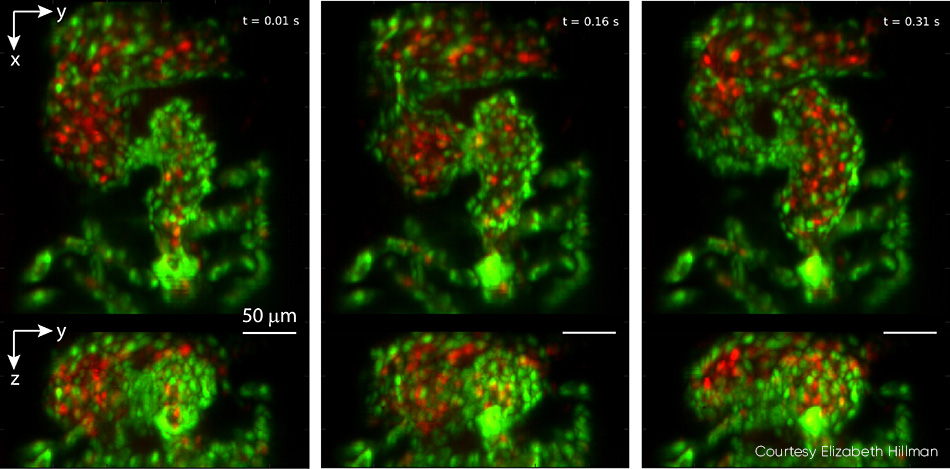
Abbildung 4:Diese Dreifachansicht stammt aus einem Echtzeit-Video des Herzschlags eines Zebrafisches, das mit einer Bildrate von 100 Bildern pro Sekunde aufgenommen wurde. Das obere Bild zeigt die z-Projektion, das untere die x-Projektion. In den aufeinanderfolgenden Bildern beginnt sich der Ventrikel zusammenzuziehen,die Ausflussklappen öffnen sich und das Herz wird anschließend vom Vorhof gefüllt. Die Endothelzellen der Herzwand sind mit EGFP (grün) markiert, während die Erythrozyten mit DsRed (rot) markiert sind. Beide Fluorophore werden mit einem 488-nm-Laser angeregt (Leistung auf der Probe: 0,6 mW). Ausführliche Informationen (einschließlich Videos) finden Sie in der Studie von V. Voleti et al. [2]
Zusammenfassung
Im gesamten Bereich der Biowissenschaften können Forscher mithilfe der Fluoreszenzmikroskopie Vorgänge auf molekularer, zellulärer, organischer und organismischer Ebene miteinander verknüpfen. Die Möglichkeit, hochauflösende mehrfarbige (3D-)Bilder zeitlich fortlaufend aufzuzeichnen (4D-Mikroskopie), ist nun bereit, eine entscheidende Rolle bei der Beschleunigung dieser Forschung zu spielen.
Literaturverzeichnis
Literaturverzeichnis
1. M. B. Bouchard et al.,Nat. Photonics, 9, 2, 113–119 (2015).
2. V. Voleti et al.,Nat. Methods, 16, 10, 1054–1062 (2019).
3. C. Dunsby,Opt. Express, 16, 25, 20306–20316 (2008).
4. R. Vaadia et al.,bioRxiv, 467274 (2018).
5. E. M. Hillman et al.,Curr. Opin. Neurobiol., 50, 190–200 (2018).
6. L. Xu et al.,Science, 368, 6487, eaaz5390 (2020).