Erfolgsgeschichten unserer Kunden
Zweiphotonen-Metabolismus-FLIM mit einem Coherent Axon
Die Becker & Hickl GmbH, ein technologischer Vorreiter im Bereich der Photonenzählgeräte, hat bereits zuvor gezeigt, dass kompakte Femtosekunden-Faserlaser als kostengünstige Anregungsquelle für Multiphotonen-Fluoreszenz-Bildgebungssysteme eingesetzt werden können. Laser mit einer Emissionswellenlänge von 780 nm, einer Pulsrate von 40 MHz bis 80 MHz und einer Durchschnittsleistung von 100 mW bis 500 mW eignen sich nicht nur zur Anregung von NAD(P)H, sondern auchauch für verschiedene andere Fluorophore [1, 2] mit sehr kurzer Fluoreszenzlebensdauer [3, 4, 5] geeignet.
Aus diesem Grund interessierten sich Becker und Hickle dafür,wieAxonbeiAxonAnwendungen funktioniert.

Abb. 1:Coherent Axon
Systemarchitektur
Als Testsystem wurde das bh DCS-120 MP Multiphotonen-FLIM-System verwendet. Die Architektur dieses Systems ist in Abbildung 2 dargestellt.
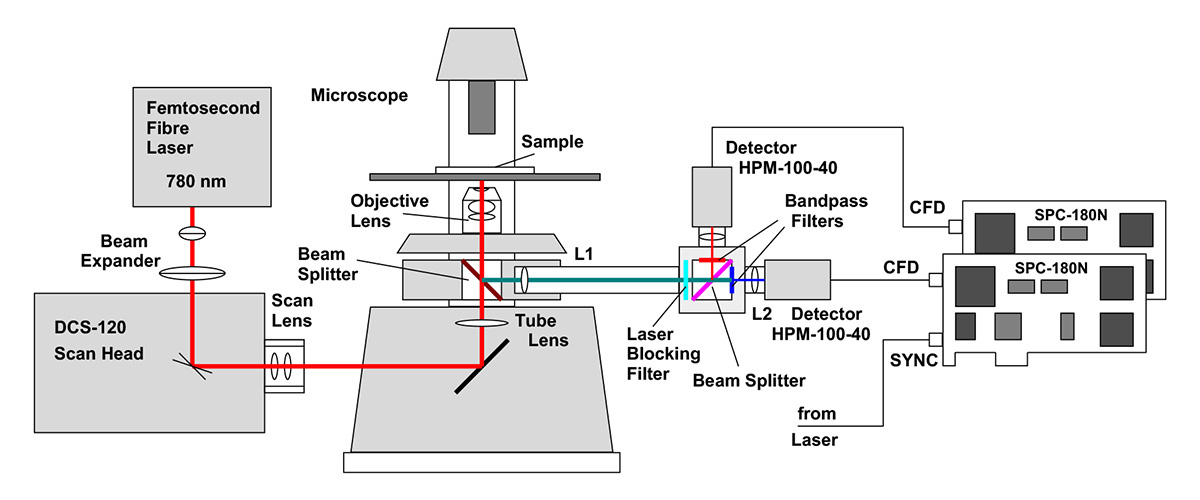
Um die maximale räumliche Auflösung zu erzielen, ist es wichtig, dass der Laserstrahl die hintere Apertur der Mikroskoplinse vollständig ausfüllt. Bei den üblichen Brennweiten von Scanner- und Tubuslinsen wird dies nicht automatisch erreicht.Daher wird der Strahl vor dem Eintritt in den Scanner um das 1,5-Fache vergrößert. Der Strahldurchmesser an der hinteren Öffnung beträgt etwa 12 mm und reicht aus, um die Öffnung selbst der größten Mikroskopobjektive auszufüllen. Eine Überfüllung der Öffnung ist unproblematisch. Da der Laser mehr Leistung liefert als erforderlich, sind Verluste bei der Anregungsleistung akzeptabel.
Das von der Probe ausgehende Fluoreszenzlicht wird durch die Mikroskoplinsen gesammelt und über einen nicht ablenkenden Strahlengang weitergeleitet. L1 und L2 bilden ein Periskop. Außerdem werden auch Photonen erfasst, die von den Mikroskoplinsen nicht vollständig kollimiert werden, beispielsweise solche, die auf ihrem Weg durch die dicke Probe gestreut werden.Das Fluoreszenzlicht wird in zwei Wellenlängenbereiche aufgeteilt und von zwei HPM-100-40-Hybriddetektoren erfasst [6, 7]. Die Einzelphotonenimpulse der Detektoren werden von zwei SPC-180N-TCSPC/FLIM-Modulen aufgezeichnet [1].Die SPC-180N-Module bestimmen die Detektionszeit der Photonen nach dem Anregungsimpuls sowie die Position des Scanners zum Zeitpunkt der Photonendetektion. Diese Informationen werden zur Erstellung von FLIM-Bildern verwendet. Dabei handelt es sich um Pixel-Arrays, wobei jedes Pixel eine vollständige Fluoreszenzabklingkurve über zahlreiche Zeitkanäle enthält [1].
Das Scannen und das Ausblenden des Laserstrahls in der Rücklaufphase werden durch die bh GVD-140-Scan-Controller-Karte hardwaremäßig gesteuert.Die Steuerung der Laserintensität erfolgt über den AOM-Steuersignaleingang des Axon-Lasers. Dieses Signal wird ebenfalls von der GVD-140-Karte bereitgestellt. Das gesamte System wird von der SPCM-Datenerfassungs- und Steuerungssoftware [1] von bh betrieben und bietet ein vollständig integriertes FLIM-System mit Scannersteuerung, Lasersteuerung, Datenerfassung und Datenanalyse. Die Benutzeroberfläche des FLIM-Systems ist in Abbildung 3 dargestellt.
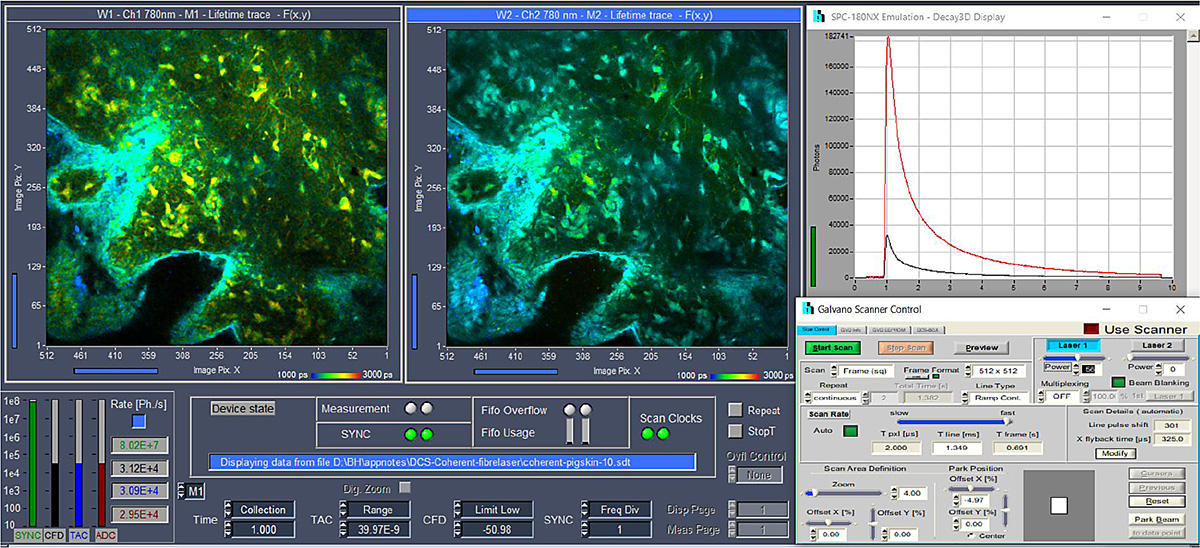
Ergebnis
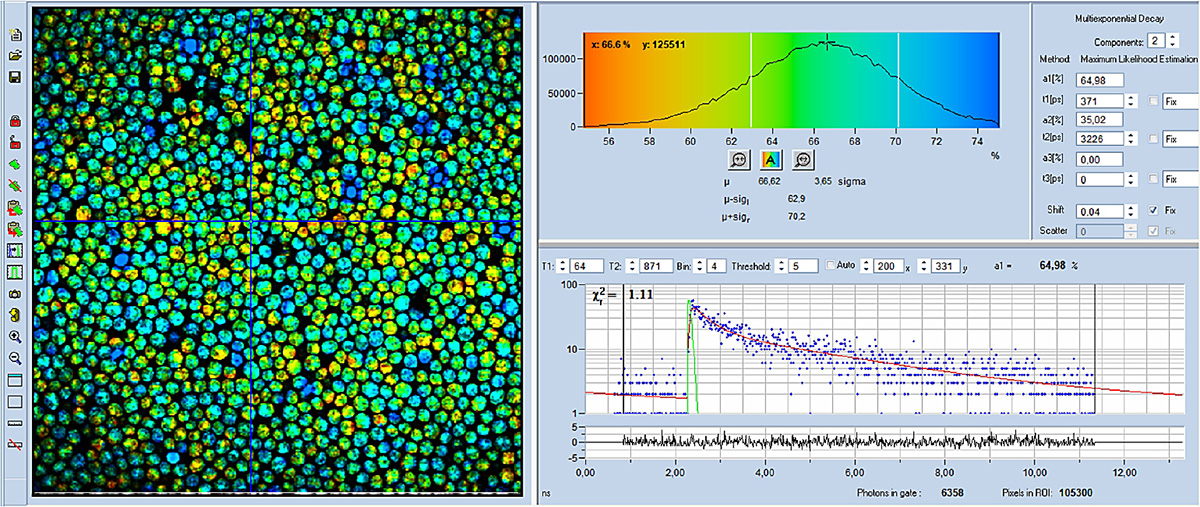
Die mit der Kombination aus DCS-120 und AXON aufgenommenen FLIM-Bilder sind in den Abbildungen 4 bis 6 dargestellt. Für alle Bilder wurde ein Ölimmersionsobjektiv mit 40-facher Vergrößerung und einer numerischen Apertur (NA) von 1,3 verwendet. Die Datenanalyse erfolgte mit der bh SPCImage NG FLIM-Datenanalysesuite. Die Abbildungen 4 und 5 zeigen farbcodierte FLIM-Bilder der mittleren (amplitudengewichteten) Lebensdauer und des Stoffwechselindikators a1.Das Histogramm des ausgewählten Bildparameters (tm oder a1) wird oben rechts angezeigt, die Abklingkurve an der Cursorposition unten rechts. Die Abklingparameter des ausgewählten Spots werden ganz rechts angezeigt.
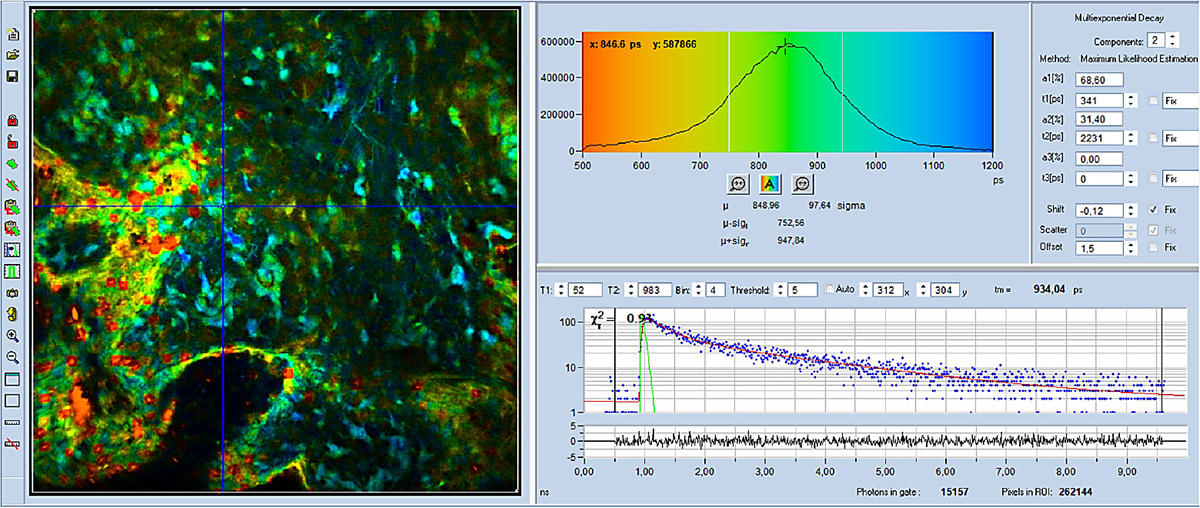
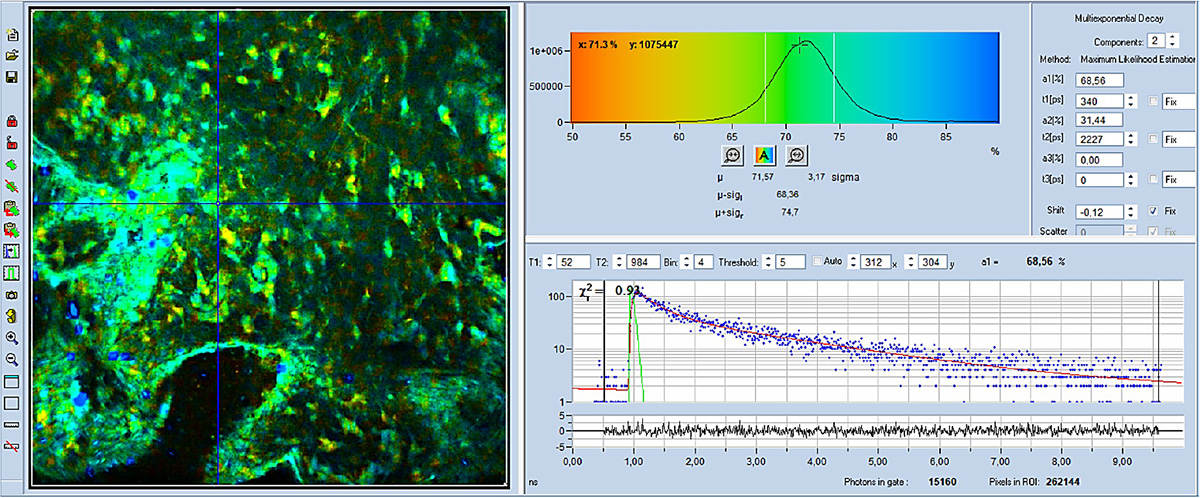
Wie Sie sehen können, unterscheidet sich a1 deutlich von Zelle zu Zelle. Dies zeigt, dass der Stoffwechselzustand von Zelle zu Zelle variiert. Ein hoher a1-Wert (blau dargestellt) deutet auf einen eher glykolytischen Stoffwechsel hin. Ein niedriger a1-Wert (gelb) deutet auf einen eher oxidativen Stoffwechsel hin.
Quellenangaben
- W. Becker, Das TCSPC-Handbuch. 10. Auflage. Becker & Hickl GmbH (2023), www.becker-hickl.com.
- W. Becker, C. Junghans, H. Netz, Zwei-Photonen-FLIM mit Femtosekunden-Faserlaser. Anwendungshinweise, www.becker-hickl.com
- W. Becker, C. Junghans, A. Bergmann: „Two-Photon FLIM of Mushroom Spores“ deckt ultraschnelle Abklingkomponenten auf. Anwendungshinweis (2021), www.becker-hickl.com
- W. Becker, A. Bergmann, C. Junghans, Ultraschnelle Fluoreszenzabklingkurven natürlicher Carotinoide. Anwendungshinweis, www.becker-hickl.com (2022)
- W. Becker, C. Junghans, V. Shcheslavskiy, „Hochauflösendes Multiphotonen enthüllt den ultraschnellen Fluoreszenzabklingvorgang im menschlichen Haar“. Anwendungshinweis, www.becker-hickl.com (2023)
- W. Becker, B. Su, K. Weisshart, O. Holub: FLIM- und FCS-Detektion bei Laser-Rastermikroskopen: Effizienzsteigerung durch GaAsP-Hybriddetektoren. Micr. Res. Technol. 74, 804–811 (2011)
- Becker & Hickl GmbH, IRF-Breite unter 20 ps bei Hybriddetektoren und MCP-PMTs. Anwendungshinweis, www.becker-hickl.com
„Durch die KombinationAxon Coherent Axon , den Detektoren, der TCSPC-/FLIM-Elektronik und der Datenanalysesoftware von bh konnten wir nachweisen, dass sich damit genaue Informationen über den Stoffwechsel lebender Zellen und Gewebe gewinnen lassen.“
– Wolfgang Becker, Geschäftsführer der Becker & Hickl GmbH, Berlin, Deutschland

