Kundenreferenzen
Zweiphotonen-Metabolismus-FLIM unter Verwendung des Coherent Axon -Faserlasers
Die Becker & Hickl GmbH, ein technologischer Marktführer im Bereich der Photonenzählgeräte, hat bereits früher gezeigt, dass kompakte Femtosekunden-Faserlaser als kostengünstige Anregungsquelle für Multiphotonen-Fluoreszenz-Bildgebungssysteme eingesetzt werden können.Die Laser haben eine Emissionswellenlänge von 780 nm, eine Pulsfrequenz von 40 MHz bis 80 MHz und eine durchschnittliche Leistung von 100 mW bis 500 mW. Sie eignen sich nicht nur zur Anregung von NAD(P)H, sondern auch für eine Vielzahl anderer Fluorophore [1, 2], darunter auch solche mit extrem kurzer Fluoreszenzlebensdauer [3, 4, 5].
Daher möchten Becker & Hickl wissen, Axon Faser-Femtosekundenlaser von Axon in diesen Anwendungen.

Abb. 1:Coherent Axon Femtosekundenlaser
Systemarchitektur
Als Testsystem verwendeten sie das Multiphotonen-FLIM-System bh DCS-120 MP. Der Aufbau des Systems ist in Abbildung 2 dargestellt.
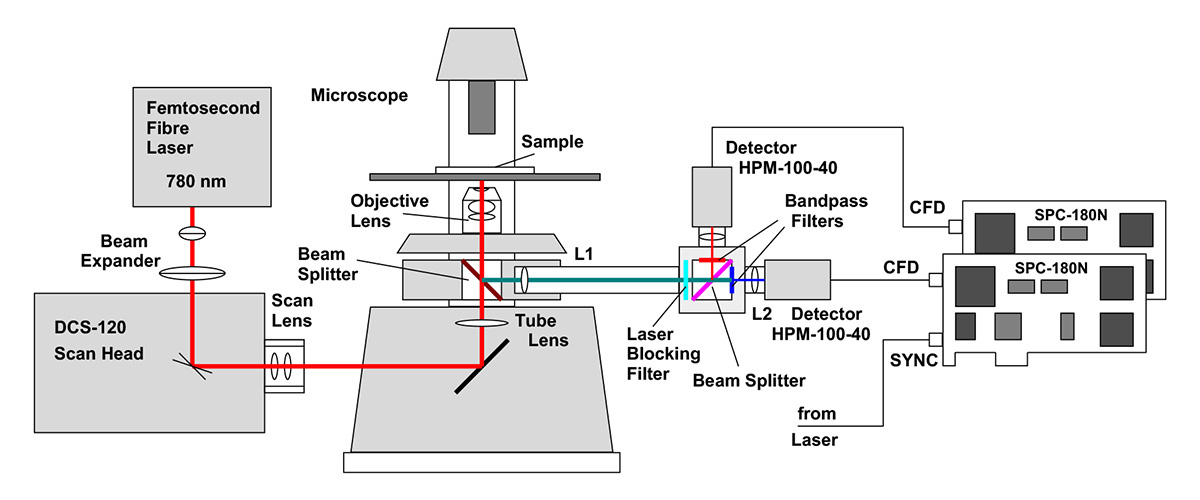
Um eine maximale räumliche Auflösung zu erzielen, muss der Laserstrahl die hintere Apertur der Mikroskoplinse vollständig ausfüllen. Bei den üblichen Brennweiten von Abtast- und Tubuslinsen ist dies nicht automatisch der Fall.Daher wird der Strahl vor dem Eintritt in den Scanner um das 1,5-Fache aufgeweitet. Der Strahldurchmesser in der hinteren Apertur beträgt etwa 12 mm, was ausreicht, um selbst die Apertur der größten Mikroskopobjektive auszufüllen. Eine Überfüllung der Mikroapertur ist unproblematisch. Die damit verbundenen Verluste an Anregungsleistung sind tolerierbar, da die vom Laser gelieferte Leistung die benötigte Leistung bei weitem übersteigt.
Die von der Probe emittierte Fluoreszenz wird von der Mikroskoplinse zurückreflektiert und anschließend über einen nicht-abtastenden Strahlengang weitergeleitet. L1 und L2 bilden ein Teleskop. Das Teleskop fängt zudem Photonen ein, die von der Mikroskoplinse nicht vollständig kollimiert wurden, beispielsweise solche, die außerhalb der dicken Probe gestreut wurden. Die Fluoreszenz wird in zwei Wellenlängenbereiche aufgeteilt und von zwei bh HPM-100-40-Mischdetektoren erfasst [6, 7]. Die Einzelphotonenimpulse der Detektoren werden in zwei SPC-180N-TCSPC/FLIM-Modulen aufgezeichnet [1]. Die SPC-180N-Module bestimmen den Zeitpunkt der Photonendetektion nach dem Anregungsimpuls sowie die Position des Scanners zum Zeitpunkt der Photonendetektion. Diese Informationen werden zur Erstellung von FLIM-Bildern verwendet. Dabei handelt es sich um Pixelarrays, wobei jedes Pixel eine vollständige Fluoreszenzabklingkurve über eine große Anzahl von Zeitkanälen enthält [1].
Die Abtastung des gegenphasigen Laserstrahls und die Strahlunterdrückung werden hardwaremäßig von der bh GVD-140-Abtaststeuerungskarte gesteuert. Die Steuerung der Laserintensität erfolgt über den AOM-Steuersignaleingang Axon . Dieses Signal wird ebenfalls von der GVD-140-Karte bereitgestellt. Das gesamte System wird von der SPCM-Datenerfassungs- und Steuerungssoftware von bh 【1】 betrieben und bietet ein vollständig integriertes FLIM-System mit Funktionen zur Scannersteuerung, Lasersteuerung, Datenerfassung und Datenanalyse. Die Benutzeroberfläche des FLIM-Systems ist in Abbildung 3 dargestellt.
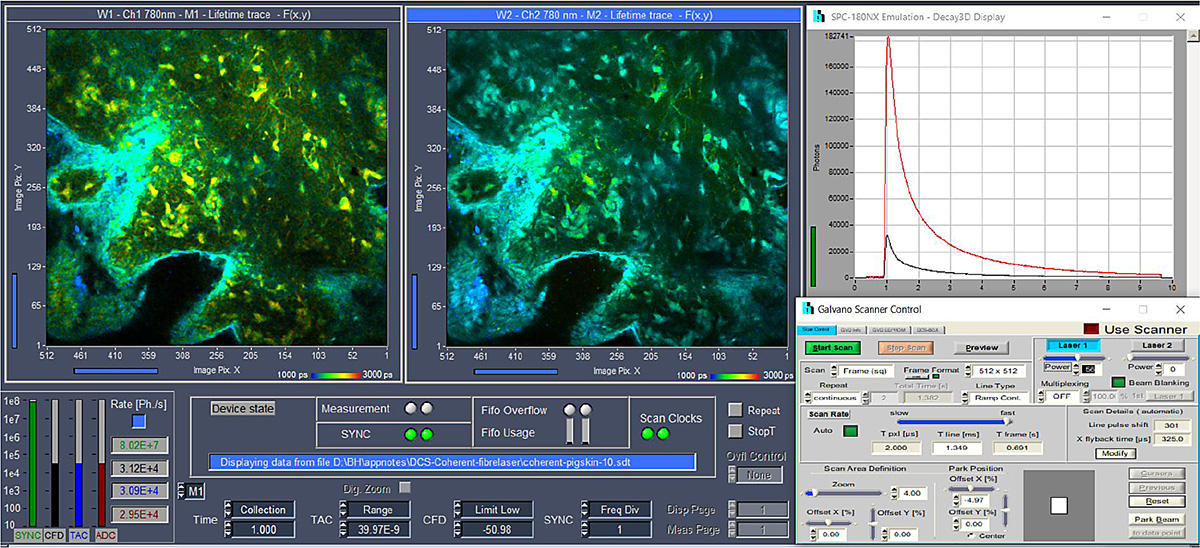
Ergebnis
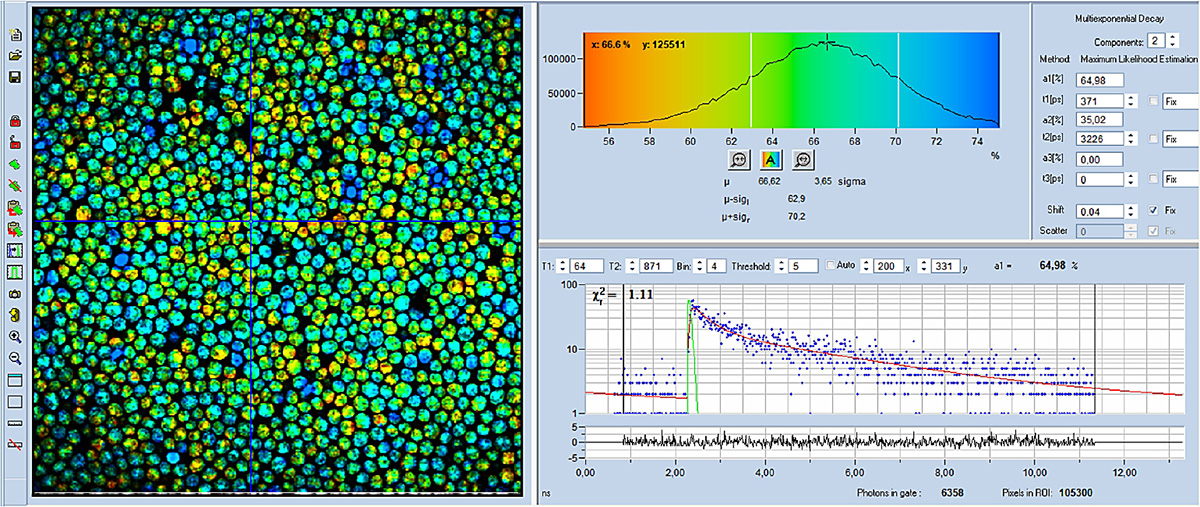
Die mitAXON FLIM-Bilder sind in den Abbildungen 4 bis 6 dargestellt. Alle Bilder wurden mit einem 40-fachen Ölimmersionsobjektiv (NA = 1,3) aufgenommen. Die Datenanalyse erfolgte mit dem bh SPCImage NG FLIM-Datenanalysepaket.Abbildung 4 und Abbildung 5 zeigen farbcodierte FLIM-Bilder der mittleren (amplitudengewichteten) Lebensdauer und des Stoffwechselindikators a1. Oben rechts ist ein Histogramm der ausgewählten Bildparameter (tm oder a1) dargestellt, unten rechts die Abklingkurve an der Cursorposition. Die Abklingparameter des ausgewählten Bildausschnitts werden ganz rechts angezeigt.
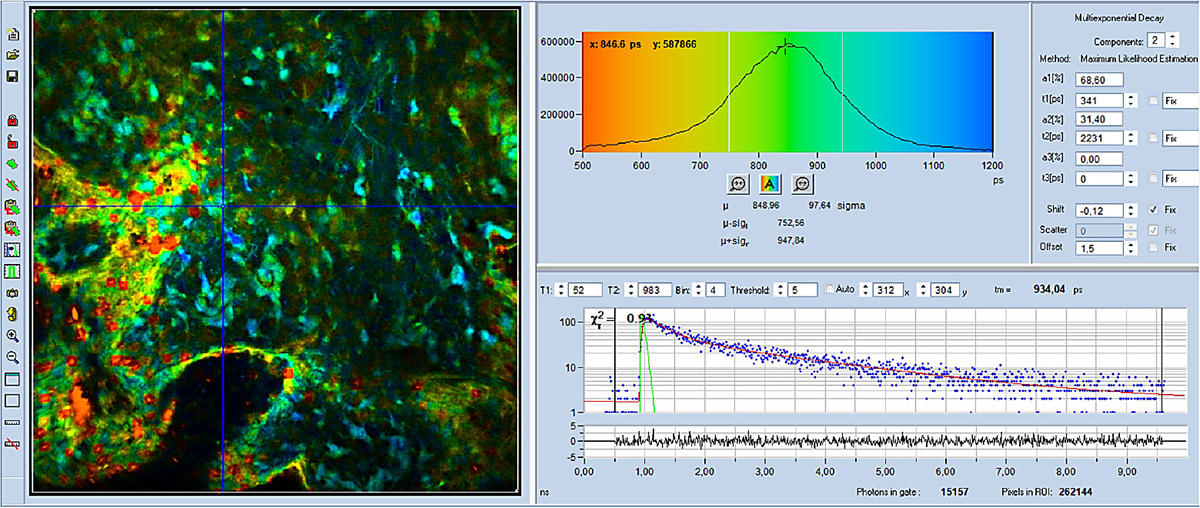
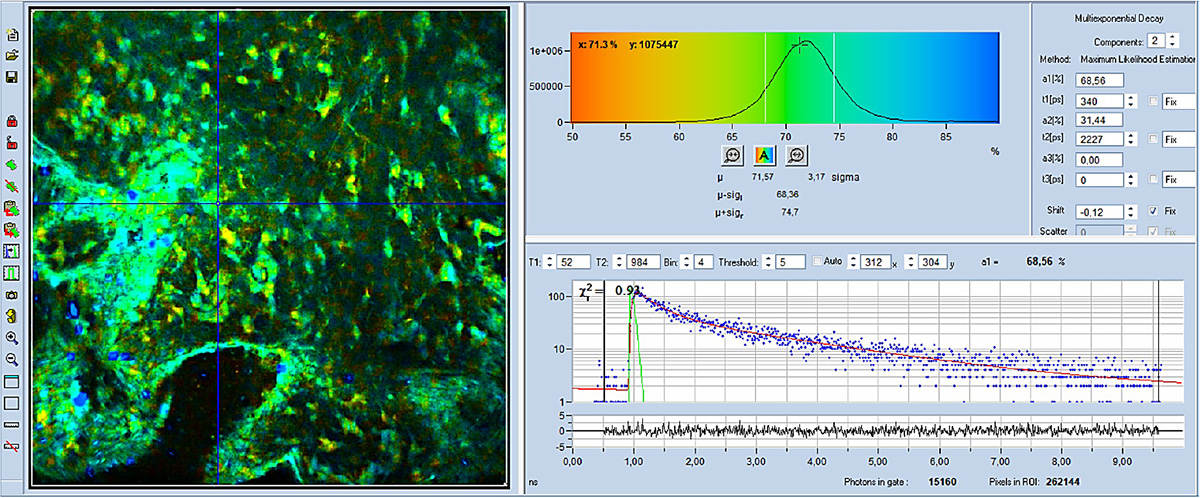
Es ist ersichtlich, dass sich a1 in den verschiedenen Zellen deutlich unterscheidet. Dies deutet darauf hin, dass der Stoffwechselzustand in den verschiedenen Zellen unterschiedlich ist. Ein hoher a1-Wert (blau dargestellt) steht für einen stärker glykolytisch geprägten Stoffwechsel, während ein niedriger a1-Wert (gelb) auf einen stärker oxidativen Stoffwechsel hindeutet.
Literaturverzeichnis
- W. Becker, bh TCSPC-Handbuch. 10. Auflage. Becker & Hickl GmbH (2023), abrufbar unter www.becker-hickl.com, gedruckte Exemplare sind bei bh erhältlich
- W. Becker, C. Junghans, H. Netz: Zwei-Photonen-FLIM mit Femtosekunden-Faserlaser. Anwendungshinweise, abrufbar unter www.becker-hickl.com
- W. Becker, C. Junghans, A. Bergmann: Zwei-Photonen-FLIM an Pilzsporen enthüllt ultrakurze Zerfallskomponenten. Anwendungsbericht (2021), abrufbar unter: www.becker-hickl.com
- W. Becker, A. Bergmann, C. Junghans, Ultrakurze Fluoreszenzabklingzeiten in natürlichen Carotinoiden. Anwendungshinweise, www.becker-hickl.com (2022)
- W. Becker, C. Junghans, V. Shcheslavskiy: Hochauflösende Multiphotonen-FLIM-Messungen enthüllen ultraschnelle Fluoreszenzabklingvorgänge im menschlichen Haar. Anwendungsbericht, www.becker-hickl.com (2023)
- W. Becker, B. Su, K. Weisshart, O. Holub, FLIM- und FCS-Laserscanning-Mikroskopie: GaAsP-Hybriddetektoren steigern die Effizienz. Micr. Res. Technol. 74, 804–811 (2011)
- Becker & Hickl GmbH: IRF-Breite von unter 20 ps bei Mischdetektoren und MCP-PMTs. Anwendungshinweise sind unter www.becker-hickl.com verfügbar.
„Wir haben gezeigt, dass der Femtosekunden-FaserlaserCoherent Axon in Kombination mit den präzisen Scanneroptiken, Detektoren, TCSPC-/FLIM-Elektronikkomponenten und der Datenanalysesoftware von bh genaue Informationen über den Stoffwechsel lebender Zellen und Gewebe liefert.“
– Wolfgang Becker, Becker &“ Geschäftsführer der Hickl GmbH

